

肺線維症になると、肺が固くなり、ガス交換ができなくなることで、呼吸器不全が起きます。しかし、これまで原因はよく分かっておらず、進行性の疾患として、早い人では3週間ほどで亡くなってしまう人もいました。現在は特効薬もなく、進行を遅らせる程度の治療しかできません。しかし、私たちの長年の研究で、肺の線維化のメカニズムがほぼ見えて参りました。皆様の御寄附を活用し、新しい治療薬の開発を目指します。
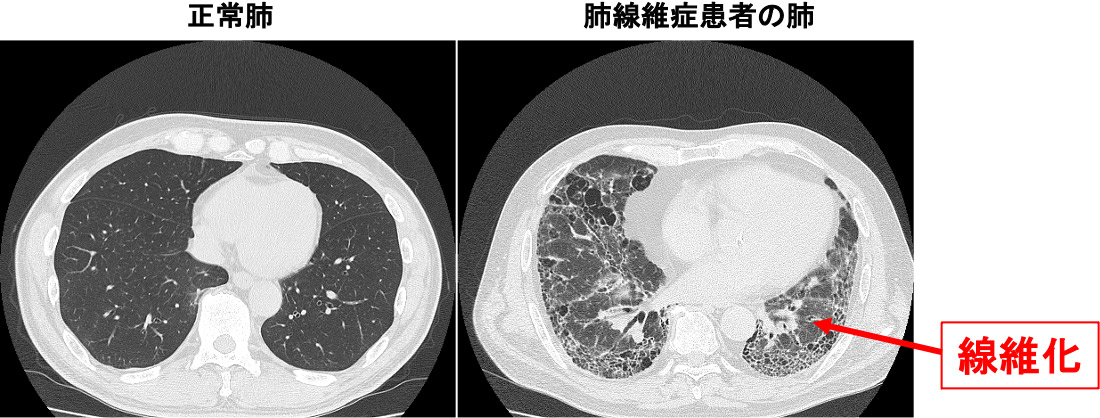
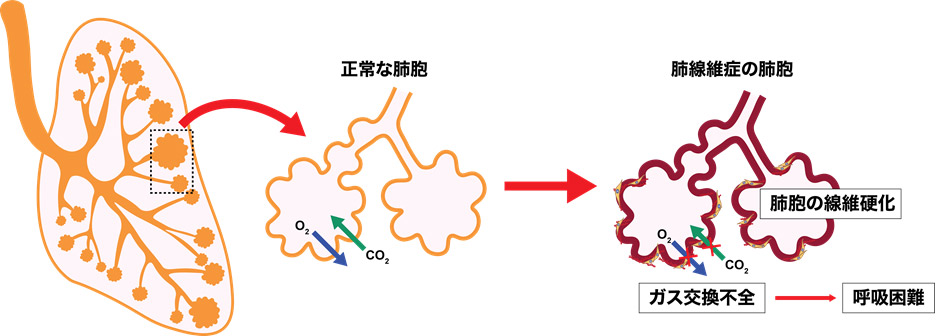
健康な人の肺では、肺胞に傷がついてもその傷は修復され、ガス交換は問題なく維持されます。しかし、肺胞が長期間繰り返し傷ついたり、粉塵にさらされたり、ウィルスや真菌などの感染症を発症したりしてしまうと、それを治そうとする働きによって過剰なコラーゲン線維などが肺胞の壁に蓄積されます。その結果、空気の通り道が狭くなり、硬くなるという線維化が起きると考えられています。肺が線維化すると、肺が十分に膨らまなくなり、ガス交換ができずに酸欠状態になるため息苦しくなります。肺の線維化は新型コロナウィルス感染による肺炎や、間質性肺炎といった様々な病気に合併します。しかしながらステロイドや免疫抑制剤といった対症療法しか治療の選択肢がなく、有効な治療が確立されていないことが問題点です。
千葉大学の私たちの研究室では、長年世界を先駆けて肺線維症の研究をしております。ここから先は少し難しい話になりますが、私たちは肺組織に浸潤する組織常在性記憶CD4⁺T細胞を見つけ、その一部は線維化を引き起こす病原性の高い細胞集団であるということを発見しました。最近は幹細胞であるⅡ型上皮細胞からⅠ型上皮細胞への分化移行が、傷害肺の機能回復に重要であるということも報告されています。そして、この分化移行が破綻することが、線維化の原因です。この分化移行のメカニズムはこれまでよく分かっていなかったのですが、私たちはCD4⁺T細胞がこれに深くかかわっていることをつきとめました。そのメカニズムを、最新の技術を用いて解明することが今回の研究です。根本的な病態が解明できることで、根本治療薬の創薬が可能となります。
ここで、非常に難しい言葉が出てきたので少しご説明させていただきます。
肺胞は、必要な酸素を取り込み不要な二酸化炭素を出すガス交換を行うために、Ⅰ型、Ⅱ型の肺胞上皮細胞という細胞に覆われています。Ⅰ型肺胞上皮細胞は主にガス交換を行う役割を持っており、Ⅱ型上皮細胞は界面活性剤のようなものを分泌し、肺がつぶれることを防ぎます。Ⅱ型は自分をコピーしたり、何らかの原因によってⅠ型が死んでしまった際にそれを補うために自らがⅠ型に変身(分化移行)することができます。この分化移行がうまくいかないことで線維化が起きています。今回Single cell RNA-seqという最新の技術を用いて細胞を1細胞レベルで詳細に解析していき、根本的な病態解明を目指します。


私たちの長年の研究成果で、もう線維化を引き起こしている役者は分かっています。あとは、今回皆様からのご寄付を活用してSingle cell RNA-seqを使って複数のからみあった病態をほぐして解析をしていくだけです。
根本的な病態が分かれば、分子標的薬という根本治療薬の創薬につながります。一日でも早く治療を確立させるために、皆様の御支援を活用していきたいと思います。この度は本当にありがとうございました。

千葉大みらい医療基金では、寄付をする際に寄付金の活用先を任意の領域や研究に指定することができます。この研究をご支援頂けます場合は、「免疫発生学」とご指定ください。